Lipide und Tenside
Fette
Zusammensetzung und Aufbau der Fette
Fette sind Ester aus Glycerin und Fettsäuren. Diese Säuren sind langkettige Carbonsäuren. In Fetten kommen folgende Fettsäuren häufig vor:
Fettsynthese
Die Fettsynthese ist eine Esterreaktion zwischen den Hydroxygruppen des Glycerins und der Carboxylgruppe der Säuren. Dabei werden drei Wassermoleküle abgespalten, das weitere Produkt bezeichnet man als Triacylglycerin:
Man spricht von einem einfachen Triacylglycerin, wenn die drei Reste gleich sind, also zum Beispiel nur Palmitinsäure sind; von einem gemischten Triacylglycerin ist die Rede, wenn mindestens einer der Reste verschieden ist. Fette sind dabei immer Gemische dieser zwei „Arten“.
Eigenschaften
Öle enthalten mehr ungesättigte Fettsäuren als feste Fette (niedrigerer Schmelzbereich) aufgrund der geringeren zwischenmolekularen Kräfte und vor allem wegen der Struktur (Z-Konfiguration). Der Schmelzpunkt wird durch die Masse und durch die Zahl der Doppelbindungen beeinflusst.
| Fettsäure | Schmelzpunkt |
| Palmitinsäure | 63 °C |
| Stearinsäure | 70 °C |
| Ölsäure | 13 °C |
| Linolsäure | –5 °C |
| Linolensäure | –11 °C |
Die Z-Konfiguration bedingt dabei einen Knick in der Molekülkette, wodurch eine regelmäßige Anordnung in einem Feststoffgitter erschwert wird. Deshalb sind ungesättigte Fettsäuren bei Raumtemperatur flüssig (vgl. Tab. 1).
Mit der Iodzahl kann man angeben, ob in einem Fett viel oder wenig Fettsäuren vorhanden sind. Sie gibt an, wie viel Gramm Iod von 100 Gramm des untersuchten Fettes gebunden werden (durch elektrophile Addition). So hat z.B. Kokosfett eine Iodzahl von 7-10, Milchfett: 33-43 und Sonnenblumenöl 125-136.
Außerdem besitzen Fette folgende Eigenschaften:
- Farblos bis gelb
- Geschmack- und geruchlos
- Geringere Dichte als Wasser
- Gut löslich in hydrophoben Lösungsmitteln (aufgrund der langen unpolaren Alkylresten)
- Bei Raumtemperatur schwer flüchtig (Fettfleckprobe)
Bei längerem Lagern unter Luft- und Lichteinwirkung tritt die unangenehme Folge auf, dass das Fett ranzig wird. Dabei laufen zwei Prozesse nebeneinander ab:
- Hydrolytische Spaltung des Fettmoleküls: Es treten freie Fettsäuren auf. Ein Maß für die Konzentration freier Fettsäuren in einem Fett ist die Säurezahl; sie gibt an, wie viel Milligramm Kalilauge zur Neutralisation von 1g Fett benötigt werden. Sie ist damit einen Hinweis auf die Frische des Fettes.
- Ungesättigte Fettsäuren werden leicht oxidiert an der Doppelbindung und nachfolgend aufgespalten. Dabei treten Bruchstücke mit unangenehmen Geruch auf.
Fetthärtung
Aus Ölen werden feste Fette:
Durch Hydrieren werden aus Pflanzenölen feste Fette gewonnen, die für die menschliche Ernährung (z.B. Margarinenherstellung) und für technische Zwecke (u.a. Seifenherstellung) herangezogen werden.
Bei der Herstellung von Fetten zur Margarinenproduktion findet eine partielle Hydrierung statt, um einen bestimmten Prozentsatz an essentiellen Fettsäuren zu erhalten.
Verwendung
Fette sind wichtig als Nahrungsmittel. So benötigt man wegen fettlöslicher Vitamine circa 60-70 Gramm Fett pro Tag. Außerdem wird damit Energie gespeichert. So kann eine Person mit einer Masse von 70 Kilogramm circa 11 Kilogramm Fett speichern, was einem Energiewert von ungefähr 400.000 kJ entspricht.
Fette bekommen aufgrund der größeren Nachfrage nach Biodiesel zusätzlich eine größer Bedeutung.
Tenside
Als Tenside (lat. tensio Spannung) werden Stoffe genannt, die die Oberflächenspannung von Wasser herabsetzen. Zu ihnen zählen Seifen und synthetische Waschmittel; letztere bezeichnet man auch als Detergentien.
Seifen
Seifen sind Natrium- und Kaliumsalze höherer Fettsäuren. Die Herstellung bezeichnet man als Fettverseifung. Verwendet man Natriumhydroxid bekommt man Kernseife, bei Kaliumhydroxid die Schmierseife.
Die Fettsäuren werden mit einem modernen Hochdruckverfahren hergestellt: Fett und überhitzter Wasserdampf reagieren bei Temperaturen von 100-250°C und einem Druck von 60 bar zu den Fettsäuren und Glycerin. Nach Abtrennung des Glycerins liegen die Ionen vor.
Eigenschaften
Die Eigenschaften der Seife werden durch den Bau des amphiphilen Seifenanions (mit dem hydrophoben Alkylrest und der hydrophilen Carboxylatgruppe) bestimmt:
- Herabsetzung der Oberflächenspannung und damit besseres Benetzungsvermögen (s. unten)
- Mizellenbildung (s. unten)
- Ablösen einer Fettverschmutzung von einer Faser
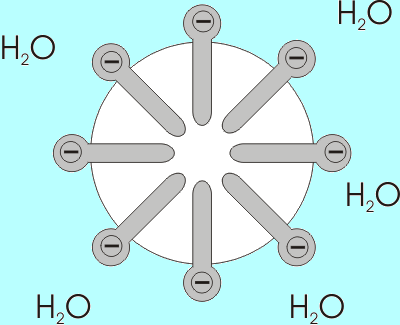
Die Umnetzung mit Seifenanionen führt dazu, dass die wasserunlöslichen Schmutzpartikel als Kerne einer Mizelle in Lösung gebracht werden. Die nach außen gerichteten negativen Ladungen verhindern durch elektrostatische Abstoßung, dass sich in Lösung gebrachte Schmutzpartikel wieder zusammenlagern oder erneut auf die Textilfasern aufziehen.
Nachteile
Durch die alkalische Reaktion der Seifenanionen mit Wasser (pH ≈ 8,5-9) ergeben sich Nachteile bei ihrer Verwendung:
- Unangenehm für die Haut durch den Angriff des Säureschutzfilms
- Schäden an alkaliempfindlichem Gewebe (z.B. Polyamide, -ester, Seide, Wolle)
- Ausfällen von Fettsäuren in sauren Milien
- Bildung unlöslicher Kalkseifen mit Magnesium- und Calciumionen
- Keine bzw. schlechtere Waschwirkung bei hartem Wasser
- Können sich im Gewebe anlagern (Folge: Gewebe kann brüchig werden)
- Kann zu allergischen Hautreaktionen führen
Synthetische Waschmittel: Anionische Tenside
Beispiele für anionische Tenside ist die Gruppe des Alkylbenzolsulfonats (ABS), die sehr schwache Basen sind. Sie besitzen zwischen acht und sechzehn Methylgruppen.
Die Vorteile dieses Tensids sind, dass der pH-Wert neutral bleibt, sich keine schwerlöslichen Kalkseifen bilden und es eine Waschaktivität auch im sauren Bereich gibt.